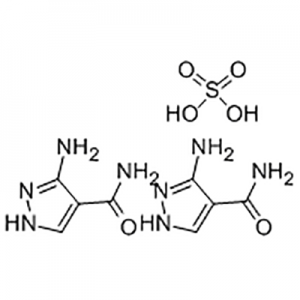
2′-మెథాక్సీ-3′-నైట్రో-బైఫినైల్-3-కార్బాక్సిలిక్ ఆమ్లం
2′-మెథాక్సీ-3′-నైట్రో-బైఫినైల్-3-కార్బాక్సిలిక్ ఆమ్లం
2'-Methoxy-3'-nitro-biphenyl-3-carboxylic యాసిడ్ ఎల్ట్రోంబోపాగ్ యొక్క మధ్యవర్తిగా ఉపయోగించబడుతుంది.
ఎల్ట్రోంబోపాగ్, UKలో గ్లాక్సో స్మిత్క్లైన్ (GSK) చే అభివృద్ధి చేయబడింది మరియు తరువాత స్విట్జర్లాండ్లోని నోవార్టిస్తో సంయుక్తంగా అభివృద్ధి చేయబడింది, ఇది ప్రపంచంలోనే మొట్టమొదటి మరియు ఏకైక ఆమోదించబడిన చిన్న అణువు నాన్ పెప్టైడ్ TPO రిసెప్టర్ అగోనిస్ట్.Eltrombopag 2008లో ఇడియోపతిక్ థ్రోంబోసైటోపెనిక్ పర్పురా (ITP) చికిత్స కోసం US FDA చే ఆమోదించబడింది మరియు 2014లో తీవ్రమైన అప్లాస్టిక్ అనీమియా (AA) చికిత్స కోసం ఆమోదించబడింది.ఇటీవలి 30 సంవత్సరాలలో AA చికిత్స కోసం US FDAచే ఆమోదించబడిన మొదటి ఔషధం కూడా ఇది.
డిసెంబర్ 2012లో, US FDA దీర్ఘకాలిక హెపటైటిస్ C (CHC) ఉన్న రోగులలో థ్రోంబోసైటోపెనియా చికిత్స కోసం ఎల్ట్రోంబోపాగ్ని ఆమోదించింది, తద్వారా తక్కువ ప్లేట్లెట్ కౌంట్ కారణంగా పేలవమైన రోగ నిరూపణ ఉన్న హెపటైటిస్ సి రోగులు కాలేయ వ్యాధులకు ఇంటర్ఫెరాన్ ఆధారిత ప్రామాణిక చికిత్సను ప్రారంభించవచ్చు మరియు నిర్వహించవచ్చు.ఫిబ్రవరి 3,2014న, ఇమ్యునోథెరపీకి పూర్తిగా స్పందించని తీవ్రమైన కెమికల్బుక్ అప్లాస్టిక్ అనీమియా (SAA) ఉన్న రోగులలో హెమోపెనియా చికిత్స కోసం ఎల్ట్రోంబోపాగ్ యొక్క పురోగతి చికిత్స ఔషధ అర్హతను FDA మంజూరు చేసిందని గ్లాక్సో స్మిత్క్లైన్ ప్రకటించింది.ఆగష్టు 24, 2015న, US FDA కార్టికోస్టెరాయిడ్స్, ఇమ్యునోగ్లోబులిన్లు లేదా స్ప్లెనెక్టమీకి తగినంత ప్రతిస్పందన లేని దీర్ఘకాలిక రోగనిరోధక థ్రోంబోసైటోపెనియా (ITP)తో బాధపడుతున్న 1 సంవత్సరం మరియు అంతకంటే ఎక్కువ వయస్సు ఉన్న పెద్దలు మరియు పిల్లలలో థ్రోంబోసైటోపెనియా చికిత్స కోసం ఎల్ట్రోంబోపాగ్ని ఆమోదించింది.జనవరి 4,2018న, ఎల్ట్రోంబోపాగ్ను ప్రైమరీ ఇమ్యూన్ థ్రోంబోసైటోపెనియా (ITP) చికిత్స కోసం చైనాలో జాబితా చేయడానికి ఆమోదించబడింది.


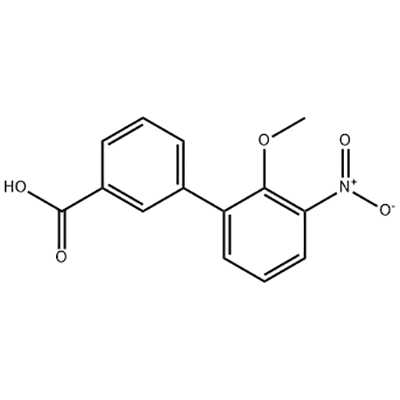

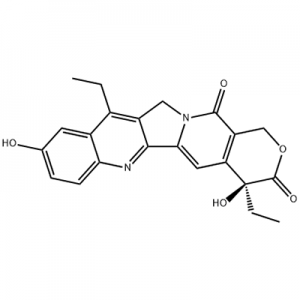
![పెంటామిథిలిన్ బిస్[1-(3,4-డైమెథాక్సిబెంజైల్)-3,4-డైహైడ్రో-6,7-డైమెథాక్సీ-1H-ఐసోక్వినోలిన్-2-ప్రొపియోనేట్], డయాక్సలేట్](http://cdn.globalso.com/jindunchem-med/image281-300x300.png)

![కాస్ప్ ఉంగిన్ అసిటేట్;కాస్పోఫంగిన్ అసిటేట్;కాన్సిడాస్;కాస్పోఫంగిన్ అసిటేట్ [USAN:BAN:JAN];](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)